La cataracte
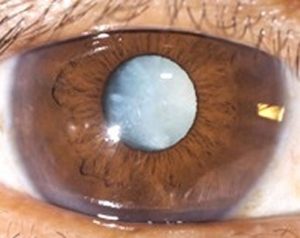
Cataracte
Le cristallin est une lentille transparente à l’intérieur de l’œil qui lui permet de voir net. Une cataracte est une opacification de ce cristallin qui survient avec l’âge. Il s’agit d’un problème très fréquent et la cataracte est une des principales causes de cécité dans le monde.
D’autre part, il peut exister des cataractes précoces chez des patients diabétiques, des cataractes secondaires à l’utilisation de corticoïdes et des cataractes liées à des maladies métaboliques. La cataracte peut aussi être causée par des traumatismes oculaires, inflammations oculaires telles que les uvéïtes et peut être également secondaire à des interventions chirurgicales intraoculaires.
Principaux symptômes:
baisse d’acuité visuelle progressive, changement de la réfraction, modification de la perception des couleurs ( jaunissement) et des contrastes ainsi qu’une sensibilité accrue à la lumière.
Rétinopathie diabétique
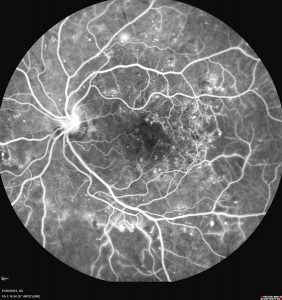
Rétinopathie diabétique
Le diabète est une maladie qui peut atteindre progressivement les petits vaisseaux du corps humain, autrement dit la microcirculation. L’œil est un organe cible du diabète, mais aussi les reins, le coeur et le système nerveux. La conséquence la plus grave du diabète dans les yeux est la rétinopathie diabétique, provoquée par la détérioration progressive des petits vaisseaux de la rétine. Cela entraîne la formation de micro-anévrismes et une atteinte de la microcirculation rétinienne. Cette atteinte peut entraîner des oedèmes et des zones entières de mauvaise circulation sanguine. Un œdème est une accumulation de liquide dans les couches de la rétine.
Lorsque cet œdème est présent dans la macula, qui est la partie centrale de la rétine (responsable de la vision centrale), il est appelé œdème maculaire.
De plus, une mauvaise circulation sanguine dans la rétine peut favoriser l’apparition de néovaisseaux. Ces néovaisseaux peuvent se rompre facilement et conduire à des hémorragies intra-oculaires appelées hémorragies du vitré, qui peuvent être responsables d’une baisse soudaine de la vision.
Une des complications tardives les plus redoutées de ces nouveaux vaisseaux est un décollement de la rétine par traction causée par ces néovaisseaux. Ces lésions mentionnées ci-dessus peuvent se produire, le plus souvent, après quelques années de diabète.
Un examen de fond d’oeil doit être réalisé 5 ans après le diagnostic d’un diabète de type 1. Pour les patients atteints d’un diabète d’apparition tardive, le diabète dit de type 2, un examen de fond d’oeil doit être réalisé au moment du diagnostic, car la date précise d’apparition du diabète peut être difficile à déterminer.
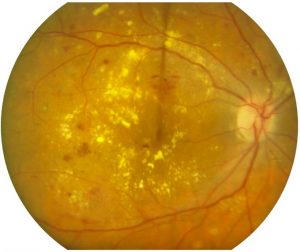
Rétinopathie diabétique
Le diabète peut causer aussi des épisodes de vision trouble non liés à une rétinopathie diabétique mais à une forte variation de la glycémie lors du diagnostic du diabète. La vision floue s’explique par un changement des dimensions du cristallin au cours des variations de la glycémie. La vue a tendance à redevenir normale quelques semaines après l’équilibre de la glycémie.
Autre complication oculaire du diabète est le strabisme, causé par une atteinte des nerfs qui contrôlent le mouvement des yeux. Ce strabisme peut être temporaire et mettre quelques mois à disparaître.
L’examen annuel de la vue avec réalisation de fond d’oeil est recommandé chez les patients atteints de diabète dans le cadre de la prévention de la rétinopathie diabétique.
Le contrôle journalier de la glycémie et des bons niveaux de l’hémoglobine glyquée sont les seuls moyens efficaces de prévenir la rétinopathie diabétique, ainsi que d’autres complications liées au diabète.
La rétinopathie des prématurés
La rétinopathie des prématurés (ROP) est une maladie qui peut toucher les bébés prématurés. Elle dépend du degré de prématurité et du poids de naissance du nouveau-né.
Le système vasculaire rétinien complète sa formation à la 36e semaine de grossesse. L’apparition de la rétinopathie des prématurés est liée à l’extension de la zone immature de la rétine de l’enfant (encore sans vaisseaux bien développés) au moment de la naissance. Cette rétine immature produit de façon excessive des facteurs de croissance tels que le VEGF (Vaso Endothelial Growth Factor) entre autres, qui provoquent l’apparition de multiples petits vaisseaux malformés et extrêmement agressifs. Ces vaisseaux rétiniens poussent brutalement vers le vitré, à l’intérieur de l’œil, provoquant une traction sur la rétine conduisant à un décollement grave et irréversible de la rétine, dont le pronostic chirurgical et visuel est mauvais, même dans les meilleurs centres mondiaux d’ophtalmologie pédiatrique.
La rétinopathie du prématuré est classée en différents stades qui varient de 1 à 5. Le facteur le plus important, selon les dernières tendances et les articles de la littérature, est la présence ou non de la Maladie Plus. La littérature tend à indiquer un traitement précoce de la ROP dès le stade 2 si la Maladie Plus est présente.
La photocoagulation à laser est le traitement de choix pour la ROP. Le traitement doit être effectué dans les 72 heures après son indication, selon les directives mondiale GCP (good clinical practice). Le traitement de la ROP par des anti-corps monoclonaux tels que les anti-VEGF est de plus en plus utilisé dans la prise en charge de ces bébés.
Le suivi post traitement est très important pour vérifier la régression de la Maladie Plus et pour décider d’un éventuel re-traitement.
Le traitement de la ROP est assuré dans des centres de néonatalogie habitués dans la prise en charge d’enfants à haut risque. Le traitement est réalisé sous anesthésie générale.
Décollement de la rétine
La rétine est un tissu qui se situe à l’intérieur de l’oeil et tapisse sa partie postérieure. La lumière et les images qui pénètrent dans nos yeux traversent toutes les structures transparentes de l’oeil et finissent par se projeter sur la rétine. À son tour, la rétine reçoit les images et les transforme en signaux électriques qui sont envoyés au cerveau par le nerf optique. Les cellules de la rétine sont appelées photorécepteurs.
Lorsqu’un décollement de rétine se produit, ses photorécepteurs entrent en souffrance et finissent par perdre leur vitalité de façon irréversible au bout de quelques jours ou quelques semaines. Le décollement de la rétine se produit lorsque une déchirure rétinienne permet le passage du liquide provenant du corps vitré (gélatine qui remplit la cavité interne de l’œil) sous la rétine créant un espace entre la rétine et la paroi de l’œil.
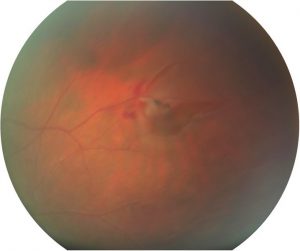
déchirure rétinienne
Le décollement de rétine peut survenir spontanément, suite à un décollement du vitré ou à un traumatisme. Les patients myopes sont particulièrement vulnérables à un décollement de rétine. Les symptômes les plus fréquemment rapportés d’un décollement de rétine sont l’apparition de flashs lumineux dans le champ de vision, la présence soudaine de taches sombres mobiles sur le champ de vision(corps flottants) et/ou l’apparition d’une grande zone de vision floue sur une partie du champ visuel. Les décollements de rétine ont pour origine une déchirure de la rétine. La prise en charge consiste en une opération ayant pour objectif de bloquer et d’obturer cette déchirure empêchant ainsi le passage du liquide provenant du corps vitré. Lors de la chirurgie, au delà du blocage de la déchirure, nous aspirons ce fluide sous rétinien qui décolle la rétine. Une fois que les photorécepteurs, les cellules de la rétine responsables de la vision, sont de nouveau collés et à plat contre la paroi de l’oeil, ils arrêtent de souffrir et peuvent éventuellement se régénérer et se remettre à fonctionner de nouveau. *
Dans l’opération du décollement, la cryothérapie ou le laser est utilisé pour traiter les déchirures rétiniennes créant une adhésion stable et de long terme autour de la déchirure. Les yeux peuvent ensuite être remplis de gaz ou d’huile de silicone pour protéger la rétine, pendant que l’adhésion autour de la déchirure cicatrise.
Décollement postérieur du vitré et /ou corps flottants du vitré (floaters)

corps-flottants devant le champ de vision
Les symptômes d’un décollement postérieur du vitré peuvent être semblables à ceux d’un décollement de la rétine. Les symptômes les plus fréquemment rapportés sont la présence de corps flottants mobiles sur le champ de vision qui suivent la direction du regard (points grisâtres, toiles d’araignée…) Ces taches peuvent être associées à la vision de flashs de lumière notamment dans la partie périphérique du champ de vision.
Les flashs lumineux se produisent lorsque le corps vitré tire sur la rétine. Notre oeil est rempli par un gel transparent, appelé le corps vitré, qui est collé aux parois internes de l’oeil, dont la rétine. Dans le processus du décollement du vitré postérieur, le corps vitré va progressivement se décoller des parois de l’oeil tel un adhésif qui se détache d’une feuille de papier. A chaque fois que le vitré tire sur la rétine, cette dernière émet un signal lumineux au cerveau. Cette traction peut déchirer la rétine et une déchirure de rétine peut, à son tour, entraîner un décollement de la rétine.
Par conséquent, lors de la présence de ces symptômes, un examen de fond d’oeil doit être réalisé.
Le décollement du vitré se produit plus fréquemment entre 50 et 60 ans. Le décollement postérieur du vitré est le résultat d’un processus naturel de vieillissement du vitré.
Dans la plupart des cas, un décollement postérieur du vitré n’a pas besoin de traitement. Les symptômes ont tendance à disparaître ou diminuer après quelques semaines ou mois. Chez les patients myopes, le décollement du vitré peut se produire plus fréquemment que chez les sujets non-myopes.
Toxoplasmose oculaire
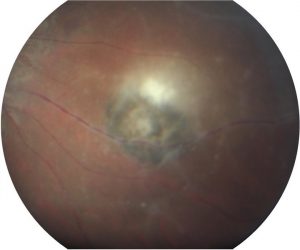
Toxoplasmose oculaire
La toxoplasmose oculaire est un type d’uvéïte (inflammation interne de l’oeil), causée par un parasite, un protozoaire, appelé Toxoplasma gondii.
L’uvée est une couche vasculaire interne de l’oeil responsable en grande partie de l’apport sanguin vers les structures intra-oculaires. Le foetus peut être contaminé in utero si sa mère a été atteinte d’une toxoplasmose aiguë pendant sa grossesse. Le patient peut alors développer une toxoplasmose oculaire seulement à l’âge adulte.
De la viande insuffisamment cuite, des aliments contaminés, de l’eau contaminée et/ou des selles d’animaux contaminées peuvent être responsables de la transmission de la toxoplasmose.
Certains fœtus peuvent être atteints d’une forme congénitale de la toxoplasmose, avec de graves atteintes de toxoplasmose oculaire. La toxoplasmose peut également entraîner des problèmes cérébraux graves pour l’enfant.
Les symptômes de la toxoplasmose oculaire sont caractérisés par une vision floue, l’apparition de corps flottants dans le champ visuel et les yeux rouges. Des douleurs oculaires peuvent également se produire. Selon la localisation du foyer d’infection dans la rétine, le patient peut avoir une vision altérée de façon permanente, comme par exemple dans des cas de toxoplasmose oculaire avec des foyers dans la macula, la partie centrale de la rétine ou à proximité du nerf optique.
La toxoplasmose peut provoquer une inflammation très intense à l’intérieur de l’œil, conduisant à une forte cicatrisation, une distorsion de la rétine ou éventuellement un décollement de la rétine. Le diagnostic de la maladie se fait par un examen ophtalmologique complet et avec confirmation par des tests sanguins (sérologie).
Le traitement actuel consiste en l’administration d’antibiotiques et d’anti-inflammatoires puissants par voie orale, afin de réduire les séquelles de l’infection.
Un traitement chirurgical n’est pas exclu si des séquelles à l’intérieur de l’oeil, entraînant à une vision floue, persistent après la résolution de l’inflammation.
Uvéite
L’uvée est une couche vasculaire interne de l’oeil responsable en grande partie de l’apport sanguin vers les structures intra-oculaires. Elle est divisée en 3 parties: l’iris, située à l’avant des yeux et responsable de la couleur des yeux; le corps ciliaire, situé derrière l’iris et qui produit le liquide qui remplit l’œil (humeur aqueuse); la choroïde, située derrière l’oeil, et en grande partie responsable de l’apport sanguin et du métabolisme rétinien. L’inflammation de cette couche est appelée uvéite.
Une uvéite peut être occasionnée par des infections et aussi par des maladies auto-immunes. Dans une partie des cas, le diagnostic n’est malheureusement pas confirmé. Une polyarthrite rhumatoïde est fréquemment à l’origine d’une uvéite antérieure.
Une cause commune d’uvéite dans la partie postérieure de l’oeil est la toxoplasmose. D’autres exemples de maladies infectieuses à l’origine d’une uvéite sont la tuberculose et la syphilis. Une uvéite peut devenir chronique, conduisant à la nécessité d’un traitement avec des médicaments immunosuppresseurs par voie orale ou injectable avec un suivi par des rhumatologues. Des maladies telles que la polyarthrite rhumatoïde, l’arthrite rhumatoïde juvénile, le Syndrome de Vogt-Koyanagi-Harada et la Sarcoïdose peuvent être à l’origine d’une uvéite. Certaines uvéites intermédiaires peuvent aussi nécessiter un traitement à long terme avec des médicaments immunosuppresseurs par voie orale ou injectables.
En cas d’uvéite, nous devons procéder à un examen complet de l’œil et à une évaluation médicale avec des bilans approfondis pour tenter de déceler l’origine de l’uvéite.
Des complications fréquentes d’une uvéite sont le glaucome et l’œdème maculaire cystoïde et l’apparition d’une cataracte.
La dégénérescence maculaire liée à l’âge (DMLA)
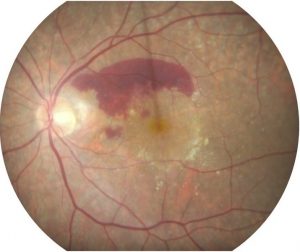
DMLA
La dégénérescence maculaire liée à l’âge, appelée DMLA, est un maladie grave de la macula (partie centrale de la rétine).
La macula correspond à la partie centrale de notre champ visuel. Elle nous procure la partie la plus riche de notre vision particulièrement celle des couleurs. Nous l’utilisons lors de la lecture ou de l’écriture ou lorsqu’on regarde le visage d’une personne devant nous.
Actuellement, cette maladie est de plus en plus répandue avec l’augmentation de l’espérance de vie. Elle est considérée comme la principale cause de baisse irréversible de la vision dans les pays développés.
Beaucoup de facteurs peuvent être impliqués dans la survenue de la DMLA. Les facteurs génétiques, la race, les facteurs environnementaux tels que le tabagisme et l’augmentation du cholestérol sont associés à la dégénérescence maculaire.
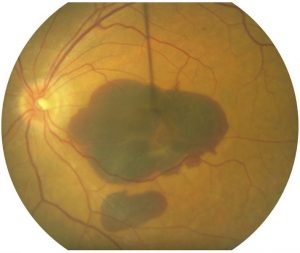
DMLA
La dégénération maculaire liée à l’âge se manifeste sous différentes formes. Le tableau peut être asymétrique entre les deux yeux. La forme la plus fréquente(85% des cas) est la sèche, caractérisée par une atrophie et par la présence de drusens. Dans la forme sèche, normalement la perte
d’acuité visuelle est lente et parfois la baisse de la vision centrale peut être légère. Néanmoins, la forme sèche peut progresser et atteindre de façon significative le centre de la macula, avec un retentissement important sur la vision centrale et de l’acuité visuelle.
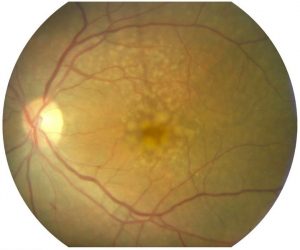
DMLA
La forme exudative(humide) représente 15% des cas et se caractérise par la présence d’une membrane de vaisseaux appelée membrane néovasculaire. Cette membrane néovasculaire pousse à partir de la choroïde et se situe sous la rétine. Cette membrane néovasculaire se développe progressivement sous la macula, provoquant un décollement localisé de rétine. La cicatrisation de la membrane néovasculaire peut entraîner une fibrose avec une perte importante de cellules responsables de la vision centrale.
Les premiers symptômes de la DMLA peuvent être une diminution lente et progressive de la vision centrale, en particulier dans les cas de DMLA sèche avec drusens ou atrophie. Les dégénérescences maculaires liées à l’âge caractérisées par des symptômes de baisse brutale de vision avec tortuosité dans les formes et les contours d’objets ou apparition d’une tache dans la partie centrale de la vision centrale sont de forme exudative (humide). Des exemples de tortuosité dans la vision centrale sont la déformation des formes d’une porte, de la surface d’une table ou d’une ligne de lettres, entre autres.
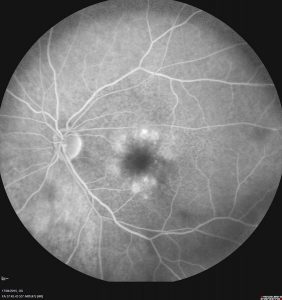
DMLA Sèche
La forme sèche de la dégénération maculaire liée à l’âge ne possède pas de traitements prouvés scientifiquement, même si l’utilisation de compléments alimentaires tels que des vitamines par voie orale peut être adoptée dans certains cas, notamment si la présence de nombreux drusens séreux et confluents est détectée.
Le patient peut s’auto-examiner par l’utilisation de la grille d’Amsler, qui est un document contenant une grille de lignes parallèles et perpendiculaires utilisée pour la détection précoce des déformations de la vision centrale causées par l’activité d’une DMLA humide.
Le traitement actuel de la forme exudative consiste en l’application d’agents anti-angiogéniques (anticorps monoclonaux) tels que l’Eylea ou le Lucentis dans l’intérieur de l’oeil. Ces agents modulent la croissance de la membrane néovasculaire et provoquent la diminution des néovaisseaux pendant quelques mois. Le traitement module la progression de la maladie diminuant l’activité métabolique des néovaisseaux. Il permet souvent une amélioration ou une stabilisation de la vision centrale. L’inconvénient du traitement consiste en la nécessité d’injections répétées . Un arrêt définitif de l’évolution de la maladie ne peut pas être garanti par le médecin. Pour une certaine partie des patients, après quelques mois ou années de traitement, l’évolution de la maladie peut cesser à moyen ou long-terme.
Membrane épi-rétinienne (MER)
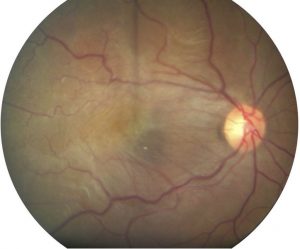
Membrane épi-rétinienne
La membrane épi-rétinienne est une fine pellicule qui se forme sur la surface de la macula. La macula est la partie centrale de la rétine. Les membranes épi-rétiniennes apparaissent le plus souvent après l’âge de 50 ans et dans la plupart des cas sont associées à un décollement postérieur du vitré. Elles sont souvent asymptomatiques et sont parfois détectées par l’ophtalmologiste au moment du fond d’oeil ou lors de la réalisation d’une tomographie à cohérence optique de contrôle.
Si le patient n’a pas de symptômes ni de baisse d’acuité visuelle et si la tomographie à cohérence optique ne montre pas de risque particulier, l’ophtalmologiste peut juste observer l’évolution de la membrane épi-rétinienne au fil du temps.
Les symptômes causés par la présence d’une membrane épi-rétinienne sont normalement d’apparition lente et progressive et caractérisés par une baisse d’acuité visuelle ou par une vision centrale avec déformations des formes et des contours des objets ou des lignes d’un livre.
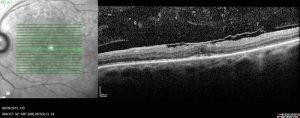
Membrane épi-rétinienne
Selon les symptômes du patient, l’atteinte de l’acuité visuelle et les caractéristiques de la membrane épi-rétinienne à la tomographie à cohérence optique, une décision pour l’ablation chirurgicale de la membrane épi-rétinienne peut être prise.
Le traitement chirurgical consiste en l’ablation de la membrane épi-rétinienne par une fine pince lors d’une vitrectomie postérieure 25 ou 27 gauges sans sutures. L’intervention dure entre 20 ou 30 minutes.
Trou maculaire
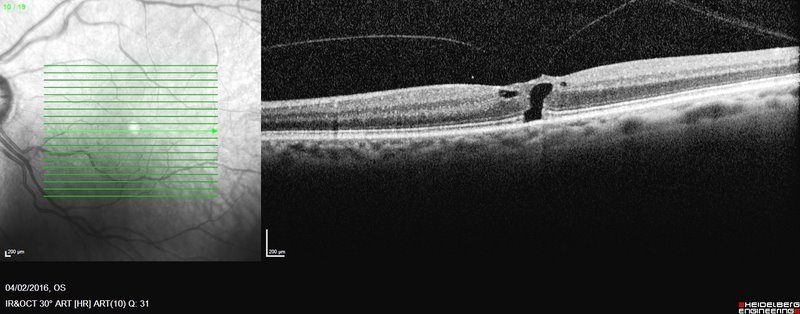
Trou maculaire en formation
Il s’agit d’un trou au niveau de la macula, qui est la partie centrale de la rétine et responsable de la vision centrale. Dans la plupart des cas, la formation de ce trou se produit spontanément. Néanmoins, l’examen de tomographie à cohérence optique montre souvent des membranes adjacentes, évoquant une membrane épi-rétinienne ou bien une traction vitréo-maculaire comme probable origine du trou.
Les premiers symptômes peuvent être l’apparition de distorsions, des ondulations ou tortuosité dans la vision centrale. Cette vision déformée se caractérise par la déformation dans la vue d’objets familiers tels qu’une porte, une table ou des lignes d’un livre. Par la suite, le tableau se caractérise par l’apparition d’une petite tache située dans le champ visuel central.
Les trous maculaires peuvent toucher l’épaisseur totale ou partielle (lamellaire) de la macula. Les trous lamellaires préservent en principe la couche de cellules visuelles de la rétine, les photorécepteurs, et provoquent dans la plupart des cas une légère à modérée baisse de vision, qui peut éventuellement être juste suivie au fil du temps par l’ophtalmologiste. Les trous complets(épaisseur totale) provoquent aussi une baisse modérée à sévère de l’acuité visuelle et ont une indication de traitement chirurgical. La chirurgie indiquée est la vitrectomie postérieure avec l’ablation des membranes vitréennes, épi-rétiniennes et rétiniennes (limitante interne). A la fin de l’intervention, l’oeil est rempli par du gaz qui, en contact avec la macula, aide à la fermeture du trou maculaire.
Le pronostic visuel pour un trou maculaire complet dépend de sa taille (diamètre), la durée de son existence et les caractéristiques anatomiques du trou observées à l’examen de tomographie à cohérence optique.
Occlusion de la veine centrale de la rétine (OVCR)
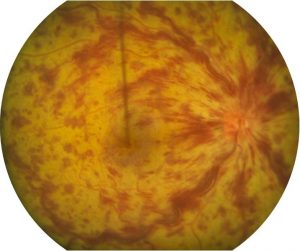
Occlusion veine centrale de retine
L’occlusion de la veine centrale de la rétine (OVCR), aussi appelée thrombose veineuse centrale de la rétine, est une interruption du flux sanguin de la veine qui effectue le drainage de la circulation rétinienne. La veine centrale de la rétine reçoit du sang provenant de 4 branches: la branche temporale-supérieure, la branche temporale-inférieure, la branche nasale-supérieure et la branche nasale-inférieure. Puisque l’occlusion se produit dans la veine centrale, les quatre branches secondaires sont touchées suite à la grande interruption circulatoire qui se propage sur tout le réseau veineux de la rétine. Le point d’interruption ou de thrombose se produit probablement dans une zone de pincement ou de rétrécissement anatomique de la veine centrale au niveau de la tête du nerf optique, dans une structure appelée de lame criblée.
Les facteurs de risque pour une occlusion de la veine centrale de la rétine sont la présence d’une hypertension oculaire ou d’un glaucome et des facteurs d’athérosclérose tels que l’hypertension, le diabète sucré, le tabagisme et la dyslipidémie (augmentation de cholestérol et de triglycérides).
Les patients remarquent généralement une baisse soudaine et rapide de la vision dans l’œil atteint. Le diagnostic est effectué au moment de l’examen de fond d’oeil. L’acuité visuelle au moment du diagnostic est considérée comme un facteur important d’évaluation de la gravité de l’occlusion et joue sur le pronostic visuel de l’oeil atteint.
L’examen d’angiographie à la fluorescéine montre une atteinte de la circulation rétinienne caractérisée par une congestion des veines rétiniennes, un possible manque de circulation sanguine dans les parties périphériques de la rétine et la possible présence d’un œdème maculaire. L’examen de tomographie à cohérence optique confirme l’éventuelle présence d’un oedème maculaire.
Des précautions doivent être prises pour éviter la survenue d’un type de glaucome appelé glaucome néovasculaire, une grave complication de l’occlusion de la veine centrale de la rétine. Cette complication apparaît normalement 3 mois après l’occlusion de la veine centrale de la rétine.
Le traitement consiste en une photocoagulation au laser diode et de possibles injections intra-oculaires si la présence d’un oedème maculaire est constatée. Le pronostic visuel est globalement mauvais. Néanmoins, dans certains cas d’occlusion de la veine centrale de la rétine avec léger retentissement sur la circulation rétinienne, nous pouvons constater une certaine préservation de la vue à long terme.
Occlusion d'une branche de la veine centrale de la rétine
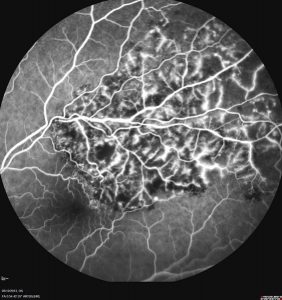
Occlusion branche veineuse rétine
L’occlusion d’une branche de la veine centrale de la rétine, aussi appelée thrombose d’une branche veineuse, est une interruption du flux sanguin d’une branche de la veine qui effectue le drainage de la circulation rétinienne. La veine centrale de la rétine possède 4 branches veineuses: la branche temporale supérieure, la branche temporale inférieure, la branche nasale supérieure et la branche nasale-inférieure.
Contrairement à l’occlusion de la veine centrale de la rétine, l’occlusion d’une branche de la veine centrale de la rétine n’a de conséquence que sur la zone de la rétine drainée par cette branche veineuse. Cette thrombose se produit fréquemment au niveau d’un point de rétrécissement de la branche veineuse situé sur l’intersection (croisement) avec une artère de la rétine.
Les facteurs prédisposant sont l’athérosclérose tels que l’hypertension, le diabète sucré, le tabagisme et la dyslipidémie (augmentation de cholestérol et de triglycérides). Le patient peut remarquer une confusion soudaine ou une baisse de vision à progression rapide dans l’œil atteint, mais si l’occlusion de la branche n’implique pas le drainage de la macula, l’occlusion peut même être asymptomatique.
Le diagnostic est effectué au moment de l’examen de fond d’oeil.
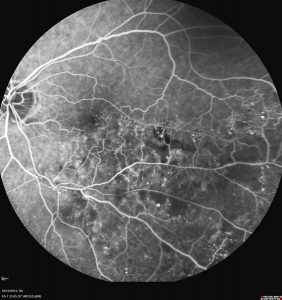
Occlusion branche veine centrale
L’examen d’angiographie à la fluorescéine montre une congestion de la branche veineuse atteinte, un possible manque de circulation sanguine dans la périphérie du quadrant rétinien impliqué et la possible présence d’un œdème maculaire. L’examen de tomographie à cohérence optique confirme l’éventuelle présence d’un oedème maculaire.
Des précautions doivent être prises pour éviter l’apparition de néovaisseaux rétiniens, un type de circulation collatérale qui peut apparaître quelques mois après l’occlusion. Ces néovaisseaux peuvent conduire à une hémorragie du vitré et/ou à un décollement de rétine par traction.
Le traitement consiste en une photocoagulation au laser de diode et de possibles injections intra-oculaires si la présence d’un oedème maculaire est constatée. Le pronostic visuel peut être mauvais si l’atteinte maculaire est significative. Néanmoins, dans certains cas d’occlusion d’une branche de la veine centrale de la rétine qui épargnent la macula, le pronostic est souvent bon si un contrôle proche est réalisé et des mesures de prévention d’une néovascularisation rétinienne sont mises en oeuvre.
Œdème maculaire
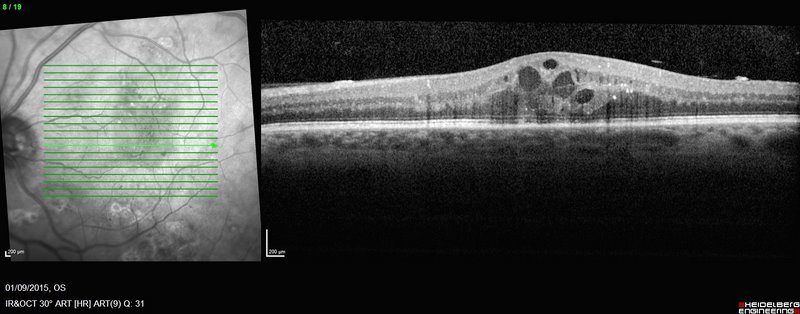
Oedeme maculaire cystoïde
L’œdème maculaire est caractérisé par la présence de fluide entre les couches de la macula, qui est la portion centrale de la rétine. Suite à une défaillance de la micro-circulation locale, du fluide s’accumule dans de petits espaces cystoïdes de la macula, conduisant à une déformation anatomique et à une souffrance de ce tissu. Un œdème chronique de longue date peut conduire à une perte de vitalité du tissu maculaire et à un mauvais pronostic visuel.
Diverses causes telles que le diabète, une DMLA (dégénération maculaire liée à l’âge), une occlusion de la veine centrale de la rétine, une occlusion d’une branche de la veine centrale de la rétine, une crise d’hypertension artérielle, une uvéite, un Syndrome d’Irvine-Gass(post-chirurgie de cataracte), des problèmes hématologiques, un décollement postérieur du vitré, un Syndrome de traction vitréo-maculaire ou un traumatisme oculaire peuvent être à l’origine du problème.
Le traitement de l’œdème maculaire doit être planifié en fonction de l’atteinte de l’acuité visuelle et de son origine.
Les injections de médicaments dans l’oeil sont très couramment réalisées actuellement. Différents types de produit tels que des anti-VEGF(Lucentis ou Eylea) ou corticoïdes de libération lente peuvent être utilisés en fonction de la cause de l’œdème.
La photocoagulation au laser peut aussi être utilisée dans des œdèmes limités et distants de la fovéa(centre de la macula).
La chirurgie de vitrectomie peut être employée dans des cas d’œdèmes associés à une traction vitréo-maculaire ou bien dans des œdèmes chroniques.
Choriorétinopathie séreuse centrale
La choriorétinopathie séreuse centrale est une maladie caractérisée par un décollement séreux (accumulation de fluide sous la macula, la partie centrale de la rétine). La couche vasculaire appelée choroïde qui se trouve en dessous de la rétine est responsable de cette fuite. La choriorétinopathie séreuse centrale peut également provoquer un décollement de l’épithélium de la rétine, appelé l’épithélium pigmentaire rétinien, qui est la couche entre la rétine et la choroïde.
De nombreuses théories tentent d’expliquer pourquoi ces fuites se produisent.
La maladie affecte les adultes de 35 à 45 ans, avec une prédominance pour le sexe masculin. La littérature médicale associe cette maladie à une personnalité appelée de type A, caractérisée par une anxiété extrême, une autocritique et une exigence envers soi même.
Les symptômes de l’apparition de la maladie sont: un trouble visuel central, une tortuosité de la vision d’objets et une possible diminution perçue de la taille des images de l’œil affecté. Des éclairs de lumière dans le centre de la vision peuvent également survenir.
La choriorétinopathie séreuse centrale est détectée par l’examen de fond d’oeil et confirmée par l’angiographie à la fluorescéine et par la tomographie à cohérence optique.
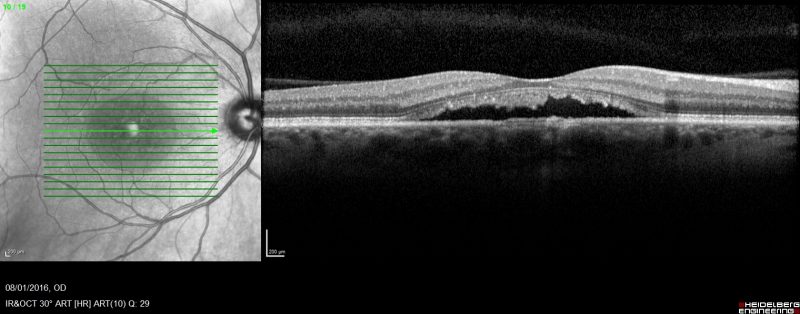
Lorsque le point de fuite est dans la partie centrale de la macula ou près d’elle, une observation ou un traitement par la photothérapie dynamique(PDT) est indiqué.
Les points de fuite peuvent être traités par une photocoagulation focale au laser de diode si les points de fuite ne se situent pas dans la vision centrale.
La prise en charge peut consister en une simple observation car la maladie s’améliore spontanément dans une bonne partie des cas et le pronostic visuel est bon, à l’exception des cas chroniques.
Glaucome
Le glaucome est une maladie qui entraîne une perte de champ visuel périphérique. Avec la progression de la maladie, une baisse de la sensibilité de la vision centrale avec diminution de sensibilité aux couleurs peut survenir.
Une lésion du nerf optique et de ses fibres nerveuses est à l’origine du glaucome. Le plus grand facteur de risque pour la lésion du nerf optique est une pression intraoculaire élevée. À l’examen du fond d’oeil, nous décelons fréquemment une augmentation de l’excavation du nerf optique.
Les valeurs normales de la PIO se situent entre 10 et 21 mmHg. La tension oculaire doit être systématiquement corrigée par la pachymétrie cornéenne.
Le glaucome chronique à angle ouvert est le type le plus commun du glaucome. Il évolue silencieusement et ne donne des symptômes que dans les stades avancés de la maladie.
Un contrôle régulier chez l’ophtalmologiste est la meilleure forme de prévention pour le glaucome.
Les examens de contrôle/suivi pour un glaucome sont le champ visuel, la tomographie à cohérence optique du nerf optique.
Le traitement actuel du glaucome consiste à diminuer la tension intraoculaire par l’utilisation de collyres hypotenseurs. Si les collyres ne réussissent pas à faire baisser la tension oculaire, d’autres options de traitement peuvent être employées telles que le laser SLT ou bien une chirurgie anti-glaucomateuse.
Glaucome aigu à angle fermé
Le glaucome aigu à angle fermé est une urgence ophtalmique. Il est caractérisé par une augmentation soudaine et importante de la tension intraoculaire, typiquement supérieure à 40 mmHg.
Les symptômes comprennent une douleur sévère, une rougeur oculaire, une vision floue, et une pupille dilatée et paralysée. La douleur est si intense qu’elle peut donner nausées et vomissements.
Les facteurs de risque pour un glaucome aigu sont la présence d’un angle étroit entre l’iris et la cornée. La fermeture de cet angle empêche le drainage de l’humeur aqueuse entrainant une soudaine hypertension oculaire.
Cet angle étroit entre l’iris et la cornée peut être causé par un cristallin de dimensions augmentées, une crête en forme de plateau dans l’iris ou bien une simple caractéristique anatomique de l’oeil.
Le traitement d’une crise de glaucome aigu consiste en l’administration de médicaments par voie intraveineuse, par voie orale, gouttes pour les yeux et finalement une iridotomie au laser YAG peut être réalisée en urgence, si la condition de l’oeil le permet.
Chez les patients ayant des antécédents de glaucome aigu à angle fermé, une petite ouverture au laser YAG peut être effectuée dans l’iris pour prévenir de futures crises de glaucome aigu à angle fermé. Ce procédé est appelé iridotomie au laser YAG.

























